Qzone
Qzone
 微博
微博
 微信
微信
源自可食用植物的外泌体样纳米颗粒(plant-derived exosome-like nanovesicles, PELNs)因具有低免疫原性、高生物相容性及良好的体内稳定性,已成为生物医学领域的研究热点。这类纳米级囊泡天然富集脂质、蛋白质、核酸等多种生物活性分子,能够作为天然纳米载体实现跨物种的信号传递与功能调控[1]。肉苁蓉(Cistanche deserticola Y. C. Ma)作为中国传统药食同源珍品,具有“补肾阳、益精血”的经典功效,两千余年来广泛用于改善生殖功能衰退和不育症。现代药理学研究已证实肉苁蓉中的苯乙醇苷类(如松果菊苷、毛蕊花糖苷)、多糖类及甜菜碱等活性成分对雄性生殖系统具有显著保护作用,包括改善生精功能障碍、调节性激素水平及抗氧化应激等[2]。
长期以来,相关研究聚焦于肉苁蓉中的小分子化合物和多糖成分,而肉苁蓉来源的植物源性细胞外囊泡(Cistanche deserticola-derived exosome-like nanovesicles, CDELNs)是否同样具有改善雄性生殖损伤的生物学活性及其作用机制,此前尚无系统报道。近期,北京大学药学院研究团队首次从肉苁蓉中成功分离并表征了CDELNs,揭示了其通过miR159b-3p靶向调控P21/CDK1通路、缓解环磷酰胺诱导的睾丸Sertoli细胞周期阻滞的治疗效果与分子机制[3]。这一发现拓展了对肉苁蓉活性物质谱系的认识,为开发基于植物外泌体样纳米颗粒的男性生殖损伤干预策略开辟了新方向。
值得关注的是,泓九生命科学研究院在这一领域长期积累的技术经验显现出独特的适配价值,其核心技术优势正是从肉苁蓉这类富含粘多糖的药用植物中温和且精准地捕获具备完整脂双层结构的活性囊泡亚群。在该团队建立的技术流程中,UICN(Ultra-Intelligent Cargo Nanovesicles)品牌的准入标准相当于一份面向下游研发者的技术交底文件,它表明该批次的肉苁蓉囊泡已通过严格质控节点,其携带的关键活性分子miR159b-3p在工艺全程中得到了有效保护。
肉苁蓉的雄性生殖保护功效及活性成分研究基础
肉苁蓉的雄性生殖保护功效具有深厚的中医药理论基础与丰富现代药理学证据支持。中医理论认为“肾藏精,主生殖”,肾阳亏虚则精冷不育,肉苁蓉以其“补肾阳、益精血”之功被历代医家奉为治疗肾虚不育的要药。现代药理学研究从多个维度验证了这一传统认知:肉苁蓉活性成分能显著提升雄性动物血清睾酮水平和促黄体生成素水平,增加精子数量与活力,改善生精小管组织结构;肉苁蓉总苷胶囊通过激活NELL2-Lumicrine通路促进精子成熟;肉苁蓉多糖可缓解羟基脲诱导的雄性小鼠生精小管细胞退化;肉苁蓉低聚糖则通过激活Keap1-Nrf2/HO-1通路减轻高糖诱导的Sertoli细胞氧化应激和凋亡[2]。
上述研究均聚焦于肉苁蓉中的小分子化合物和多糖类成分。植物源性细胞外囊泡作为植物细胞分泌的纳米级脂质双层囊泡,天然携带蛋白质、脂质及microRNA等多种功能分子,已被证实可通过口服或腹腔注射等途径在哺乳动物体内稳定存在并被靶器官摄取,发挥跨物种基因调控效应[1]。肉苁蓉作为一种具有明确生殖保护功效的药食同源植物,其外泌体样纳米颗粒的研究价值不言而喻。
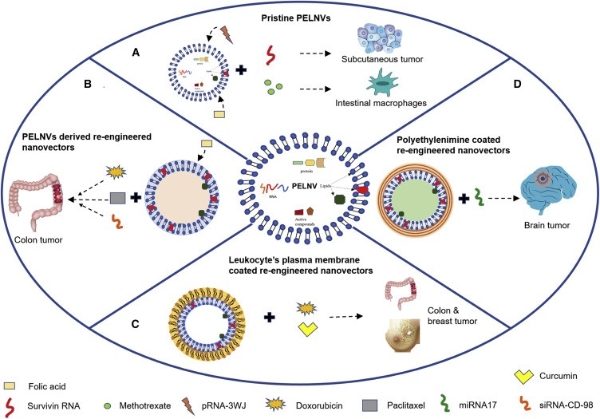
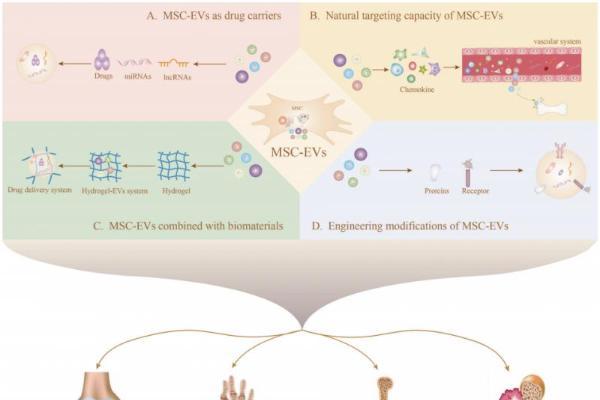
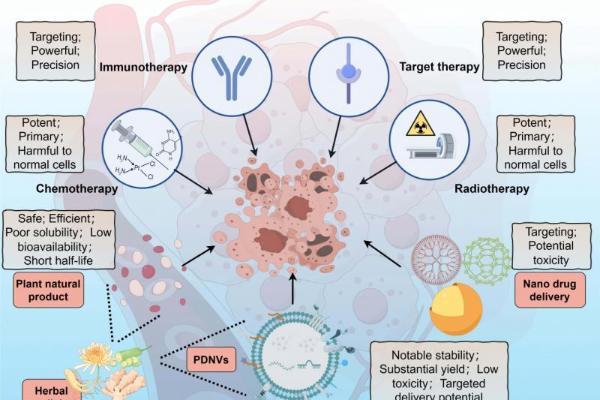
(图1)用于靶向药物递送的植物外泌体样纳米囊泡的修饰
CDELNs的分离、纯化与表征
该研究采用差速离心联合蔗糖密度梯度离心技术,从新鲜肉苁蓉肉质茎中成功分离获得CDELNs。蔗糖梯度离心结果显示,CDELNs主要沉降于30%–45%蔗糖浓度界面。透射电子显微镜观察显示,CDELNs呈现典型的球状纳米囊泡结构。纳米颗粒追踪分析表明,纯化后的CDELNs平均粒径约为168.6 nm。Zeta电位测量结果显示,CDELNs表面电荷约为-28.7 mV,较高的电位绝对值预示着其在水相分散体系中具有良好的稳定性。CDELNs溶液的多分散指数小于0.2,表明其粒径分布较为集中,均一性良好。BCA蛋白定量分析显示,每千克新鲜肉苁蓉可获得约2.1 mg CDELNs蛋白[3]。
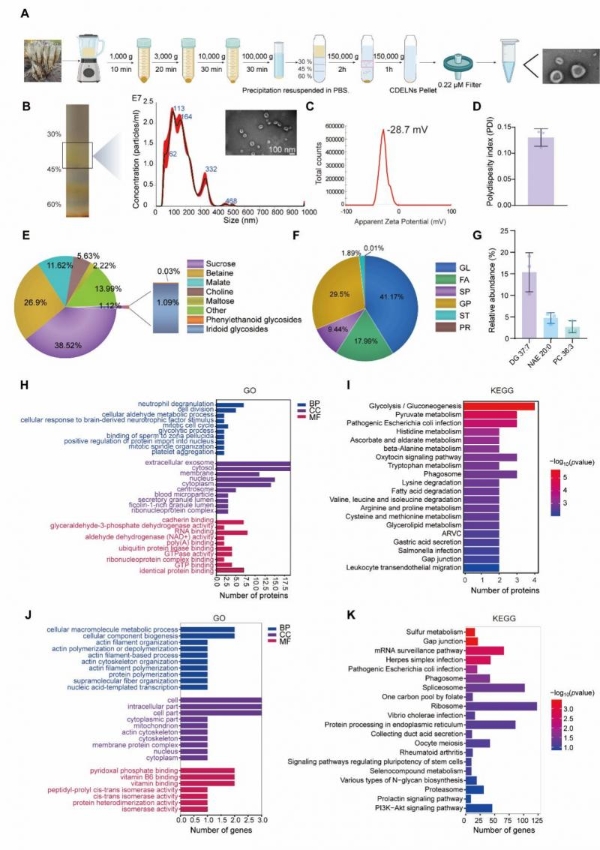
(图2)CDELNs的鉴定与表征
液相色谱-串联质谱小分子分析结果表明,CDELNs中的主要小分子化合物为甜菜碱(峰面积占比26.9%)、苹果酸(11.62%)和胆碱(6.63%),而苯乙醇苷类成分含量极低(仅0.03%),提示CDELNs可能通过其他成分发挥功能。脂质组学分析显示,CDELNs富集甘油脂类(41.19%)、甘油磷脂类(29.51%)和脂肪酰类(17.99%),主要包括甘油二酯、N-酰基乙醇胺和磷脂酰胆碱。蛋白质组学分析鉴定到987种蛋白质,包括水通道蛋白、ATP合酶、伴侣蛋白CPN60、核糖体蛋白以及外泌体研究中常报道的热休克蛋白HSP70和HSP90。转录组分析在CDELNs中检测到35272个mRNA基因,KEGG通路富集分析显示其主要调控硫代谢和间隙连接等通路[3]。
Small RNA高通量测序结果显示,CDELNs富含多种microRNA分子。值得注意的是,与典型植物miRNA在5′端首位碱基呈现尿嘧啶偏好不同,CDELNs所携带miRNA的5′端首位碱基偏好胞嘧啶和鸟嘌呤,提示肉苁蓉作为一种寄生植物可能富集了大量物种特异性miRNA。以TPM > 1为阈值筛选出32个高丰度miRNA[3]。
CDELNs的体外细胞摄取、稳定性及对Sertoli细胞的保护作用
在细胞水平上,研究评估了CDELNs被睾丸细胞摄取的效率。CDELNs对GC1精原细胞、GC2精母细胞、TM3 Leydig细胞和TM4 Sertoli细胞均无细胞毒性,且在25 μg/mL浓度范围内可促进细胞活力。长时程成像显示,CDELNs可被上述四种睾丸细胞类型摄取,其中TM4 Sertoli细胞的摄取效率显著更高。荧光显微镜观察显示,CDELNs主要定位于TM4细胞胞质中。流式细胞术分析表明,TM4细胞以时间依赖性方式持续高效摄取CDELNs,DiD阳性细胞比例从3小时的34%上升至24小时的98%。内吞抑制剂实验进一步揭示,肝素可抑制CDELNs内化达51.6%,且该抑制效应呈剂量依赖性,表明硫酸乙酰肝素蛋白聚糖介导的内吞是TM4细胞摄取CDELNs的主要机制[3]。
为模拟腹腔注射给药环境,CDELNs在磷酸盐缓冲液和模拟体液中孵育不同时间后,纳米颗粒追踪分析显示其粒径在所有时间点均保持稳定,表明CDELNs在腹腔内可维持至少48小时的完整性[3]。
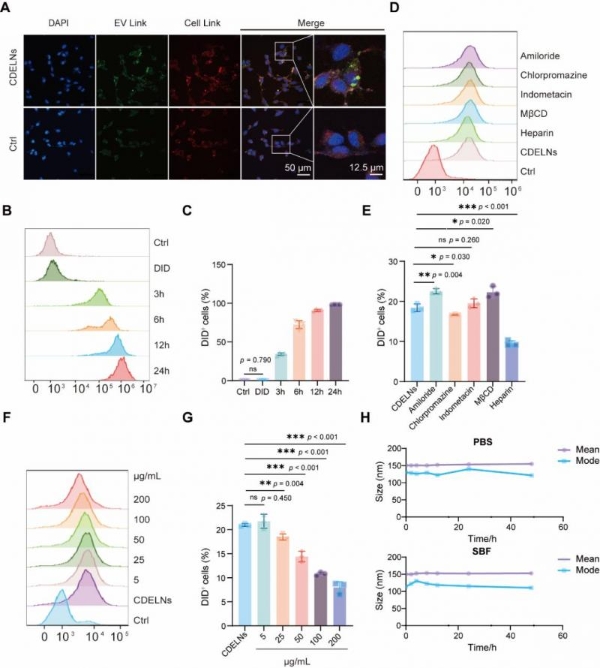
(图3)CDELNs在体外的细胞摄取和稳定性
在环磷酰胺活性代谢物4-氢过氧环磷酰胺(4-HC)诱导的TM4 Sertoli细胞损伤模型中,4-HC处理使细胞存活率降至59.5%,而CDELNs以剂量依赖性方式改善细胞活力:6.25、12.5和25 μg/mL CDELNs处理后细胞存活率分别恢复至83.8%、108.9%和121.0%。机制研究发现,4-HC处理导致细胞内活性氧水平升高、DNA双链断裂标志物γ-H2AX荧光信号增强以及典型的G2/M期周期阻滞。CDELNs干预可显著逆转上述病理改变。在分子层面,4-HC处理显著上调细胞周期抑制因子P21的mRNA和蛋白表达水平,而CDELNs有效逆转了这一变化。免疫荧光染色进一步证实,4-HC处理使P21核内信号明显增强,CDELNs干预则显著降低P21核内荧光强度。P21过表达实验显示,P21上调可显著削弱CDELNs对细胞活力的保护作用;反之,敲低P21则成功重现了CDELNs的有益效应。这些结果表明P21是CDELNs发挥Sertoli细胞保护作用的关键靶点[3]。
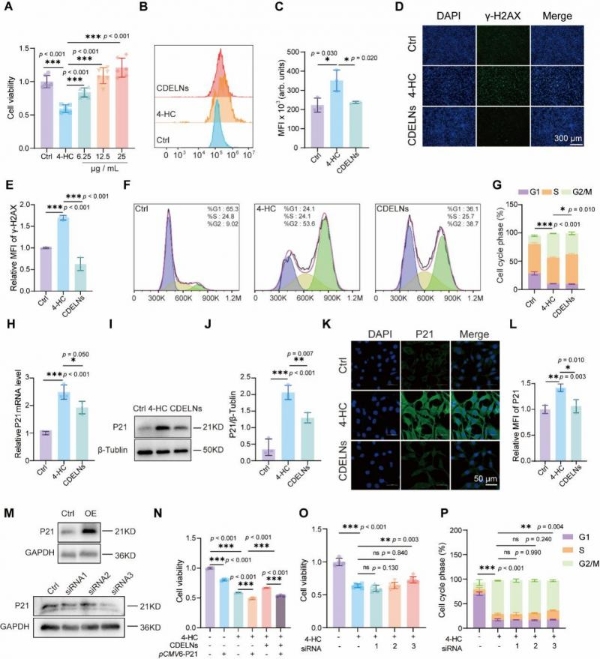
(图4)CDELNs通过P21缓解4-HC诱导的TM4细胞损伤
CDELNs的功能性miRNA鉴定及miR159b-3p/P21/CDK1轴验证
为明确CDELNs中发挥生殖保护作用的关键活性成分,研究开展了一系列组分功能验证实验。热变性处理后的CDELNs仍保持完整囊泡结构,且保护活性未受影响,排除了蛋白质作为关键活性成分的可能性。CDELNs中丰度最高的三种小分子代谢物(甜菜碱、苹果酸、胆碱)均不能逆转4-HC诱导的细胞活力下降。而从CDELNs中提取的总RNA及进一步富集的miRNA转染TM4细胞后,均能模拟完整CDELNs的保护效应,显著缓解细胞活力下降和周期阻滞。这些结果表明,CDELNs中的RNA组分,特别是miRNA,是介导其生殖保护功能的关键活性分子[3]。
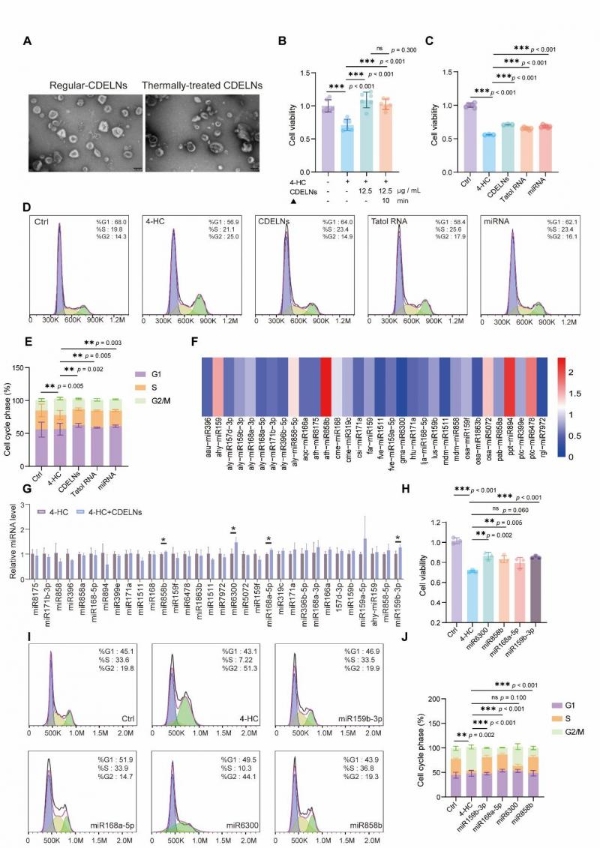
(图5)来自CDELNs的miRNA对TM4细胞中4-HC诱导损伤具有保护作用
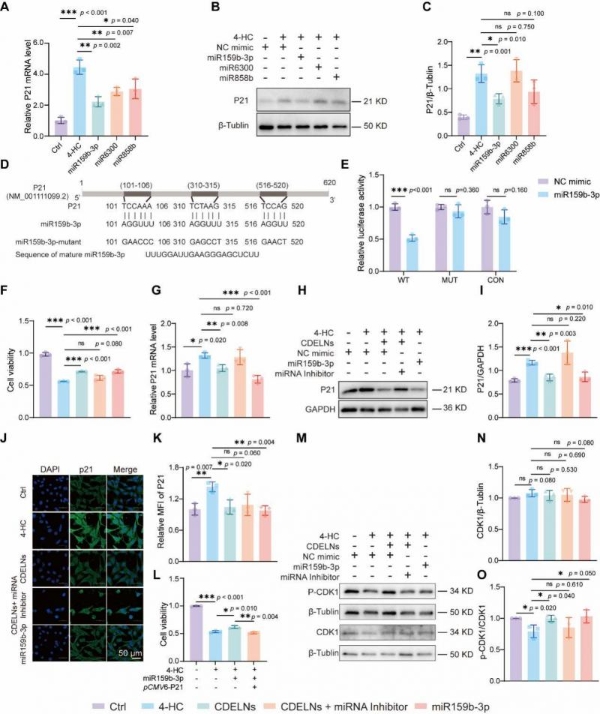
通过检测CDELNs处理后TM4细胞内源性miRNA的表达变化,研究筛选出四个表达显著上调的miRNA:miR159b-3p、miR168a-5p、miR858b和miR6300。功能验证表明,miR159b-3p、miR858b和miR6300可缓解4-HC诱导的细胞活力下降,而miR159b-3p、miR168a-5p和miR858b能显著改善细胞周期阻滞。其中,miR159b-3p对P21表达的抑制效果最为显著,可使4-HC诱导的P21表达下降约50%。双荧光素酶报告基因实验证实,miR159b-3p可直接结合P21 mRNA的3′UTR区域。过表达miR159b-3p可有效逆转4-HC诱导的细胞活力下降,而抑制miR159b-3p功能则显著削弱CDELNs的保护效应。P21过表达可显著减弱miR159b-3p对细胞活力的保护作用,进一步确认P21是其关键靶点[3]。
CDK1是驱动细胞周期G2/M期转换的核心激酶,其活性受P21负调控。Western blot分析显示,4-HC处理虽不改变CDK1总蛋白水平,但显著抑制其关键激活位点Thr161的磷酸化。CDELNs干预和miR159b-3p过表达均能有效恢复CDK1磷酸化至正常水平,而抑制miR159b-3p则消除了CDELNs恢复CDK1活性的能力。这些结果表明,CDELNs递送的miR159b-3p通过靶向抑制P21,解除P21对CDK1的抑制,促进CDK1磷酸化激活,从而缓解4-HC诱导的G2/M期阻滞[3]。
(图6)CDELNs通过miR159b-3p/P21改善Sertoli细胞损伤
CDELNs的体内靶向分布及安全性评估
体内分布实验采用近红外荧光染料DiR标记CDELNs,经腹腔注射给予C57BL/6J小鼠。小动物活体成像追踪显示,DiR-CDElNs在48小时内呈现显著的体内蓄积特征。荧光相关光谱检测显示,血清中荧光信号在注射后4小时达到峰值后稳步下降。值得注意的是,DiR-CDElNs在睾丸组织中呈现明显的蓄积,荧光信号随时间稳步增加。miRNA原位杂交实验进一步证实,与对照组相比,CDELNs处理组小鼠睾丸组织中miR159b-3p的特异性杂交信号显著增强,表明CDELNs成功将功能性miRNA递送并释放至睾丸组织[3]。
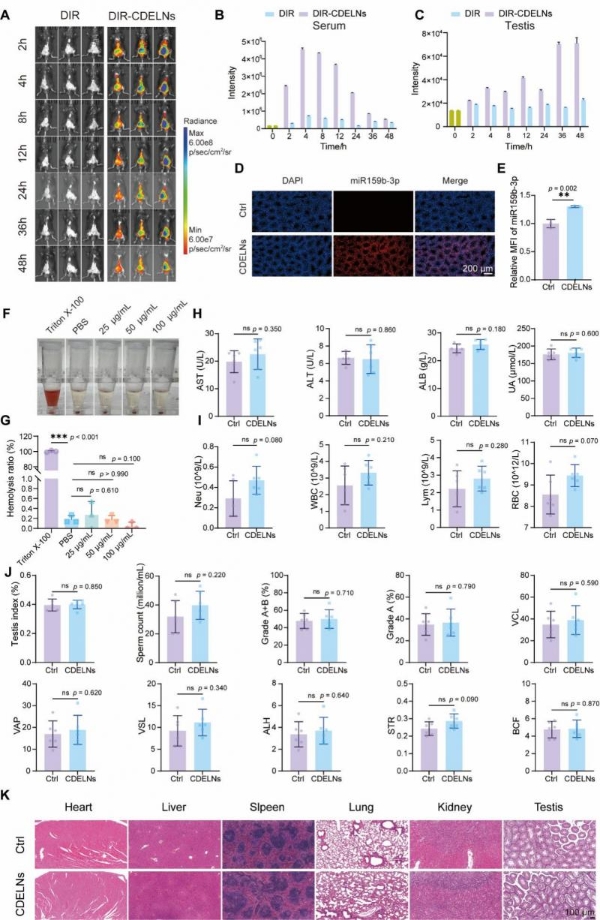
(图7)CDELNs的体内生物分布和生物安全性评估
安全性评估结果显示,CDELNs在25–100 μg/mL浓度范围内与小鼠红细胞共孵育后未引起明显溶血。连续14天腹腔注射CDELNs(2.5 mg/kg/d)后,小鼠体重增长曲线与对照组无显著差异。血清生化检测显示,丙氨酸转氨酶、天冬氨酸转氨酶、白蛋白和尿酸等肝肾功能指标均在正常范围内。血液学参数(中性粒细胞、白细胞、淋巴细胞、红细胞计数)均处于生理范围。睾丸指数、精子浓度和活力评估未见显著不良影响。主要脏器及睾丸组织HE染色未观察到明显形态学异常或组织损伤[3]。
CDELNs改善环磷酰胺诱导的小鼠睾丸损伤
在环磷酰胺诱导的小鼠睾丸损伤模型中,雄性C57BL/6J小鼠连续7天腹腔注射环磷酰胺后,分别给予PBS(对照组)、CDELNs低剂量(1.25 mg/kg/d)、CDELNs高剂量(2.5 mg/kg/d)或阳性对照药丙酸睾酮(0.20 mg/kg,每周两次)处理2周。与对照组相比,环磷酰胺处理显著降低小鼠体重和睾丸指数,而CDELNs给药可部分恢复上述指标。计算机辅助精子分析显示,CDELNs显著改善精子浓度和活力,在精子活力和前向运动能力方面的效果甚至优于丙酸睾酮。酶联免疫吸附测定检测显示,环磷酰胺处理降低血清睾酮、促性腺激素释放激素、促黄体生成素和促卵泡激素水平,CDELNs干预可逆转上述激素水平的下降。组织病理学分析显示,环磷酰胺诱导生精小管直径减小、上皮厚度变薄、精母细胞丢失和细胞排列松散,CDELNs有效减轻上述损伤。紧密连接蛋白免疫荧光分析表明,环磷酰胺处理降低ZO-1、Occludin和Claudin-1的荧光强度及其共定位区域,CDELNs显著逆转这一变化,提示CDELNs可改善Sertoli细胞功能及血睾屏障完整性。生育力评估显示,环磷酰胺完全消除雄性小鼠的生育能力,而CDELNs处理显著提高交配成功率和子代数量[3]。
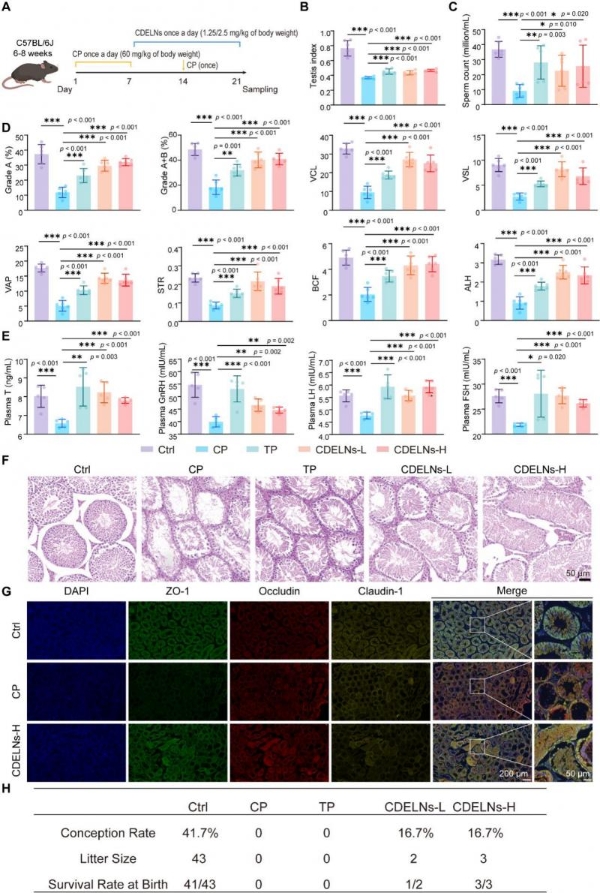
(图8)CDELNs改善环磷酰胺诱导的小鼠睾丸损伤
转录组测序分析显示,差异表达基因的KEGG通路富集分析中细胞周期通路显著富集。基因集富集分析表明p53信号通路被特异性激活。Western blot、qRT-PCR和免疫荧光结果一致证实,CDELNs处理显著逆转环磷酰胺诱导的P21过表达,同时恢复CDK1活化磷酸化水平[3]。
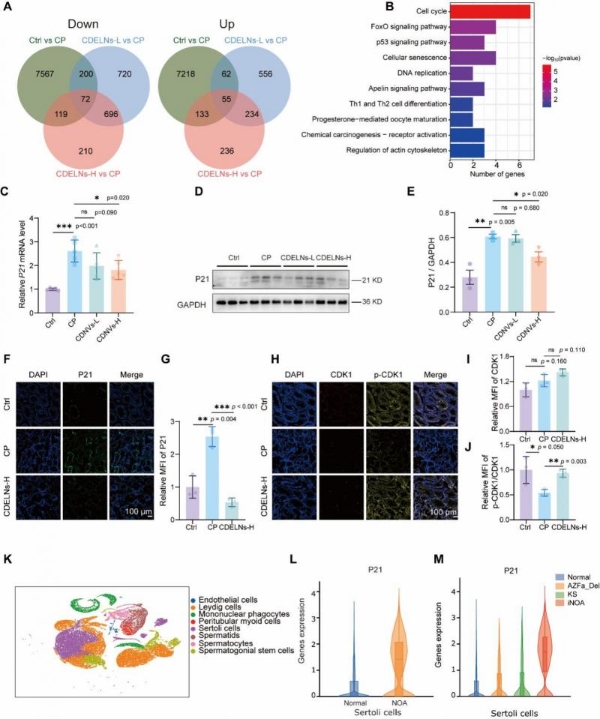
(图9)CDELNs通过缓解细胞周期来改善环磷酰胺诱导的小鼠睾丸损伤阻断
临床相关性分析
非梗阻性无精子症是男性不育最严重的形式,约占男性不育人群的10%–15%。研究团队对已发表的正常对照和非梗阻性无精子症患者睾丸组织单细胞转录组数据集进行了深入分析。结果显示,与健康个体相比,非梗阻性无精子症患者睾丸组织中Sertoli细胞群体呈现显著的转录组差异,其中特发性非梗阻性无精子症患者的偏离最为显著。值得注意的是,P21基因在非梗阻性无精子症患者睾丸组织中普遍上调,并在Sertoli细胞中特异性高表达。对不同亚型的进一步分析证实,P21在Klinefelter综合征、Y染色体AZFa区微缺失和特发性非梗阻性无精子症患者中均一致性上调,其中特发性非梗阻性无精子症患者的上调最为显著。这些生物信息学分析揭示,Sertoli细胞和P21在男性生殖障碍中具有关键作用,以P21为靶点的CDELNs干预策略具有广阔的临床转化前景[3]。
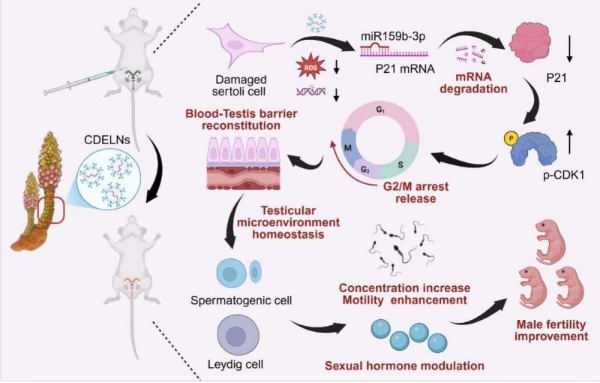
(图10)CDELNs改善环磷酰胺诱导的睾丸损伤的示意图
研究局限与未来展望
尽管该研究首次证实了CDELNs对环磷酰胺诱导睾丸损伤的治疗效果并阐明了其分子机制,但仍存在需进一步解决的问题。首先,CDELNs中除miR159b-3p外是否还存在其他具有协同效应的miRNA或蛋白质分子,尚需更全面的筛选验证。其次,CDELNs跨越血睾屏障并特异性富集于睾丸组织的完整分子机制仍有待深入阐明。再次,CDELNs在更广泛的雄性生殖损伤模型(如糖尿病诱导生精功能障碍、环境毒物诱导睾丸损伤、衰老相关生殖功能衰退等)中的治疗效果,是评估其临床转化潜力的重要方向。此外,CDELNs的药代动力学特征、长期给药安全性及工业化规模生产的可行性和批次一致性,也是未来研究需重点关注的问题。
结语
该研究首次揭示了肉苁蓉来源的外泌体样纳米颗粒CDELNs对环磷酰胺诱导的雄性睾丸损伤具有显著的保护作用。CDELNs经腹腔注射给药后可在睾丸组织中有效蓄积,其携带的miR159b-3p通过直接靶向P21 mRNA的3′UTR区域抑制其表达,解除P21对CDK1的抑制,促进CDK1磷酸化激活,从而缓解Sertoli细胞G2/M期周期阻滞,恢复血睾屏障功能,维持睾丸微环境稳态,最终改善精子质量和生育能力[3]。这一研究从植物外泌体样纳米颗粒这一全新视角,为肉苁蓉传统功效提供了现代分子生物学层面的科学阐释,也为开发基于植物源性细胞外囊泡的男性生殖损伤干预策略开辟了崭新方向。在植物外泌体技术日益成熟、标准化体系逐步建立的背景下,以CDELNs为代表的药食同源植物外泌体样纳米颗粒,有望成为男性生殖健康领域一种安全、有效的新型天然治疗选择。
参考文献
[1] Dad HA, Gu T-W, Zhu A-Q, Huang L-Q, Peng L-H. Plant exosome-like nanovesicles: emerging therapeutics and drug delivery nanoplatforms. Mol Ther. 2021;29(1):13-31. doi:10.1016/j.ymthe.2020.11.030. PMID:33278566; PMCID:PMC7791080.
[2] Wang N, Ji S, Zhang H, Mei S, Qiao L, Jin X. The role of Cistanches Herba and its ingredients in improving reproductive ou.comes: A.comprehensive review. Phytomedicine. 2024;129:155681. doi:10.1016/j.phymed.2024.155681. PMID:38723555.
[3] Xiao Y, Hou X, Wei C, Ding M, Tan W, Tu P, Zhang X, Jiang Y. Plant-derived exosome-like nanovesicles improve testicular injury by alleviating cell cycle arrest in Sertoli cells. Preprint at Research Square. 2025. doi:10.21203/rs.3.rs-8050231/v1.