
 Qzone
Qzone
 微博
微博
 微信
微信
在抗击癌症的漫长征程中,科学家们始终在寻找一种既能精准作用于病灶、又源自天然体系的高效方法。传统化疗药物在破坏细胞增殖过程中无法区分癌细胞与正常细胞,在杀伤肿瘤的同时也带来巨大副作用。许多天然活性成分也往往受制于体内分布散乱、靶向性不足等问题。如今,一项来自泓九生命科学研究院的最新研究,为这一困境带来了突破性思路:源自中药黄芪的外泌体,被首次系统证实具有显著的肝靶向性与肺靶向性,并能对肺癌和乳腺癌实现双重抑制。这意味着一类天然的“精准导航药物载体”正从传统智慧中浮现,为肿瘤治疗奠定了关键的理论与实验基础。
明确的器官趋向性:体内分布研究揭示肝肺长效滞留特性
外泌体是细胞分泌的纳米级囊泡,承担细胞间信号通讯的关键功能。然而,植物来源外泌体,特别是中药黄芪诱导产生的外泌体,进入机体后的吸收、分布、代谢等体内动力学过程尚不明确,极大地限制了其临床开发与应用。
研究团队采用高灵敏度的近红外荧光活体成像技术,实时、可视化地追踪了经染料标记的黄芪外泌体在C57小鼠体内的动态吸收、分布及清除过程。结果揭示了一条清晰的路径:黄芪外泌体可通过舌下黏膜及胃肠道迅速吸收,并在体内表现出显著的肝靶向性和肺靶向性。
更令人印象深刻的是其在靶器官中的滞留时间尤为突出。数据显示,黄芪外泌体在肝脏和肺脏中的代谢时间均长达72小时,半衰期分别为17.1±3.4小时和9.9±0.7小时,展现出显著的长效循环特性。相比之下,心脏,脾脏及肾脏并非其主要富集器官,且其消除半衰期较短。这种独特的肝、肺双靶向分布模式,并非偶然。它提示黄芪外泌体可能通过其膜表面特有的成分,被肝脏和肺组织的细胞识别,为将其开发为针对肝癌、肺癌、肝肺转移瘤的天然靶向递送系统,提供了至关重要的实验依据。
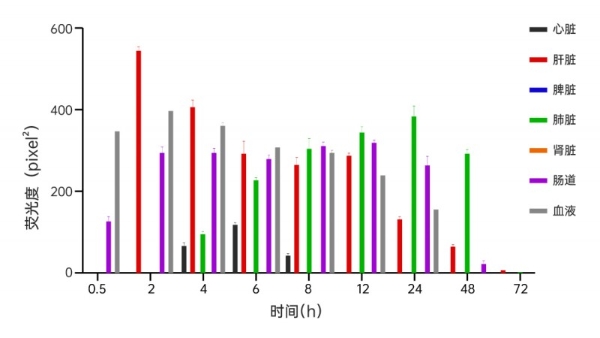
图1黄芪外泌体随时间变化图
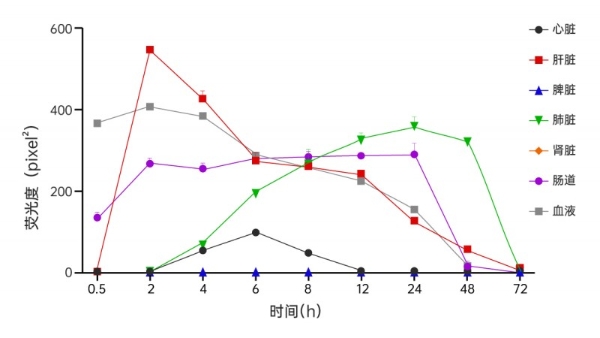
图2黄芪外泌体随时间变化图
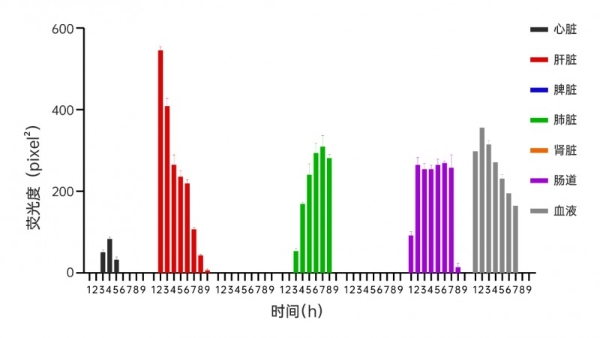
图3黄芪外泌体组织分布图
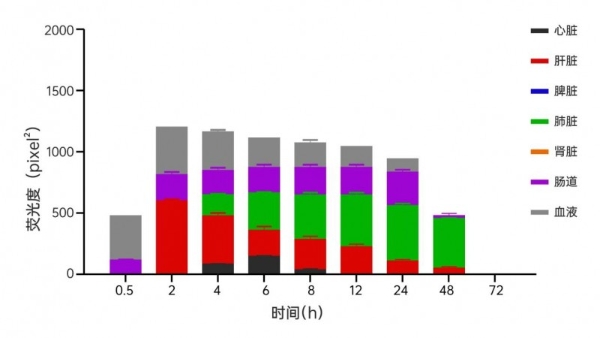
图4黄芪外泌体不同时间组织分布图
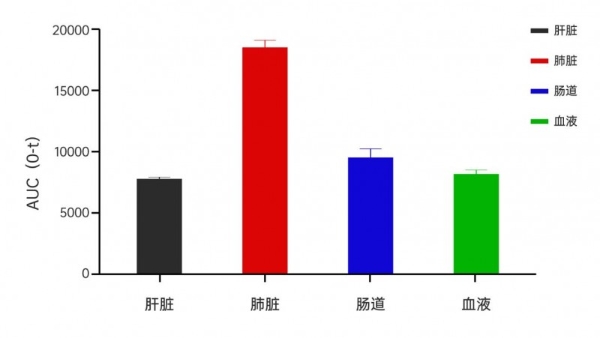
图5黄芪外泌体不同时间组织分布AUC图
同时实验结果表明,黄芪外泌体在小鼠体内的吸收率为48.63%,经肠道的吸收率为11.55%,经血液的吸收率为37.08%。这一吸收路径的明确,也为黄芪外泌体的给药方式提供了科学依据。
抑制肿瘤生长:斑马鱼模型证实对肺癌与乳腺癌的双重功效
具备了卓越的靶向潜能,黄芪外泌体自身是否具有抗肿瘤活性?研究团队利用通体透明的斑马鱼肿瘤移植模型,进行了直观验证。他们将荧光标记的人肺癌A549肿瘤细胞和乳腺癌MCF-7肿瘤细胞分别植入斑马鱼体内,构建肿瘤模型,随后用黄芪外泌体进行干预。
48小时后的荧光图像给出了震撼的结果:与未治疗的模型组相比,黄芪外泌体治疗组的肿瘤荧光信号强度急剧下降。在肺癌模型中,250、500、1000μg/ml浓度的黄芪外泌体,分别使肿瘤荧光强度降低了61.16%、74.63%和73.33%。
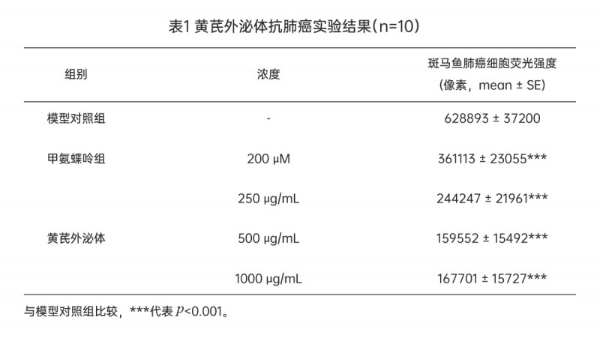
A
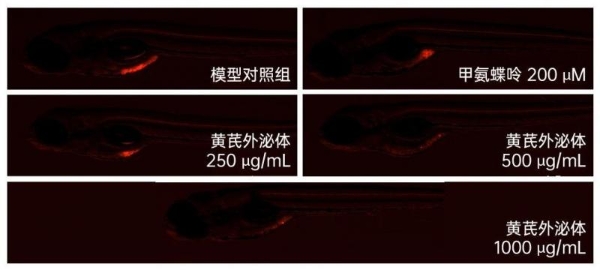
B
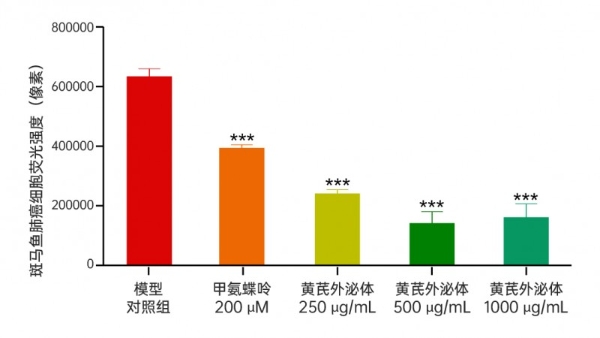
C
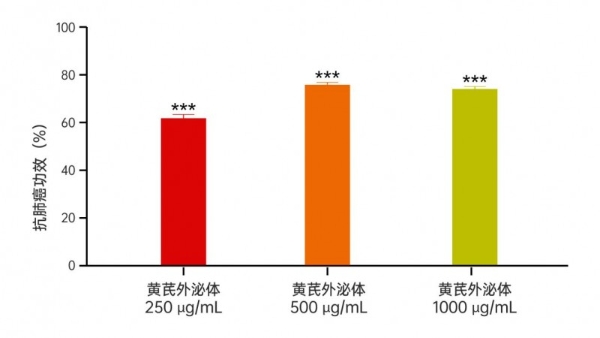
图6黄芪外泌体处理48h后斑马鱼肺癌细胞荧光强度和抗肺癌功效
A黄芪外泌体处理后斑马鱼肺癌细胞荧光强度典型图;B黄芪外泌体处理后斑马鱼肺癌细胞荧光强度(像素);C黄芪外泌体处理后抗肿瘤(肺癌)功效(%)。t检验分析方法做统计学差异:***代表p < 0.001。
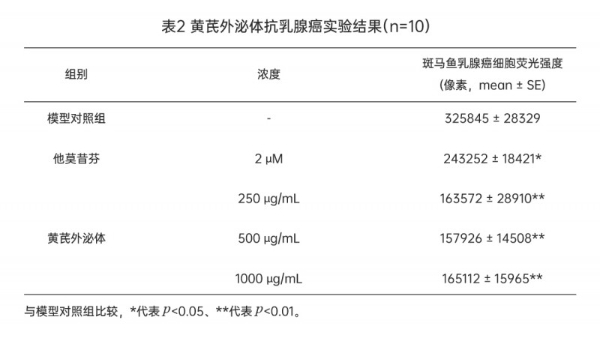
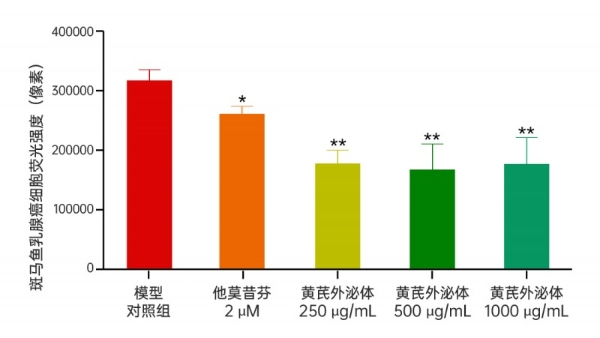
在乳腺癌模型中,同样浓度的外泌体也实现了近50%的荧光抑制率,分别降低49.80%、51.53%、49.33%。这直接证实了黄芪外泌体对两种高发恶性肿瘤细胞具有强大的抑制增殖作用。
A
B
C
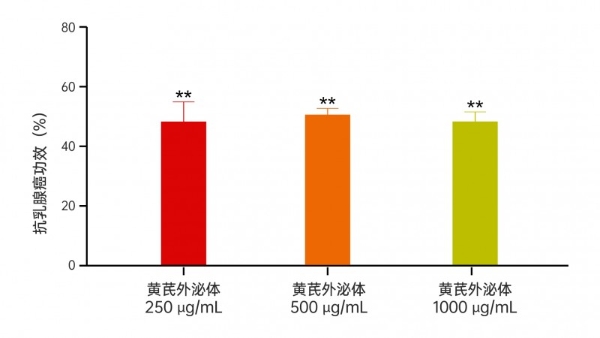
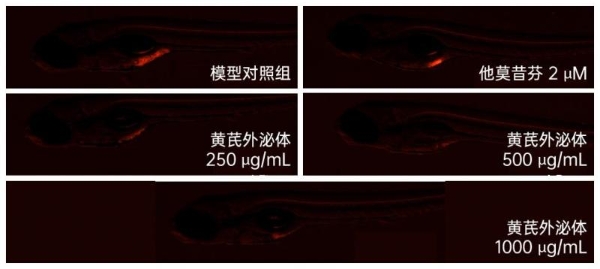
图7黄芪外泌体处理48h后斑马鱼肺癌细胞荧光强度和抗乳腺癌功效
A黄芪外泌体处理后斑马鱼乳腺癌细胞荧光强度典型图;B黄芪外泌体处理后斑马鱼乳腺癌细胞荧光强度(像素);C黄芪外泌体处理后抗肿瘤(乳腺癌)功效(%)。t检验分析方法做统计学差异:*代表p < 0.05,**代表p < 0.01。
机制探索进一步深入。基因分析发现,黄芪外泌体能够显著下调肿瘤相关炎症因子IL-6的表达,三个浓度组分别降低了23.73%、43.25%和50.66%。IL-6是肿瘤微环境中促进增殖、侵袭的关键因子,其下调从分子层面揭示了黄芪外泌体抗肿瘤活性的一个核心机制:它可能通过调节肿瘤微环境,抑制促肿瘤生长的信号通路。
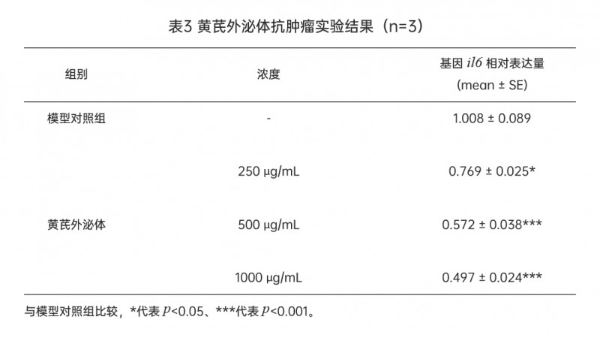
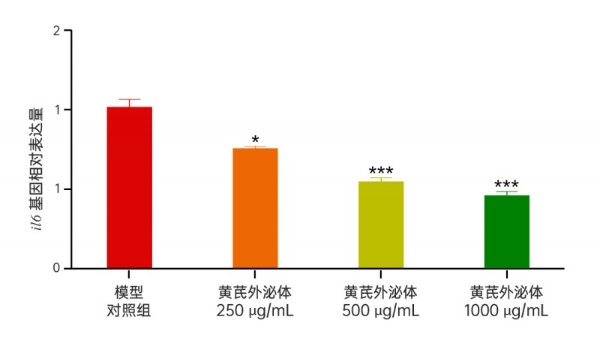
图8黄芪外泌体处理48 h后斑马鱼il6基因相对表达量
t检验分析方法做统计学差异:*代表p < 0.05、***代表p < 0.001。
天然优势与未来前景:从“补气扶正”到“精准制导”
这项研究的突破性在于,它将中医理论中黄芪“补气扶正”的宏观概念,推进到了现代纳米医学“精准制导与打击”的微观层面。与传统黄芪提取物相比,其外泌体形式具有成分明确、稳定性高、更易被细胞吸收利用的优势;与合成纳米载体相比,它又具备天然来源、免疫原性低、生物相容性极佳的特性。
黄芪外泌体明确的肝肺靶向性,为治疗原发性肝癌、肺癌以及各类癌症的肝肺转移灶提供了绝佳的递送平台。未来,科学家甚至可以进一步将其工程化,装载特定的化疗药物或核酸药物,实现精准联合治疗。
当前研究展现出的双重靶向与双重抑制潜力,足够令人振奋。它不仅仅是发现了一种新的活性成分,更是开创了一种药食同源与现代生物纳米技术相融合的研发范式:利用机体自身及天然产物的智慧通讯系统——外泌体,去实现更精准、更温和、更系统的治疗。
从清晰的体内靶向分布到确切的肿瘤生长抑制,黄芪外泌体的研究展示了传统药源与现代纳米医学技术相结合的巨大潜力,为肿瘤治疗领域开辟了一条值得深入探索的新途径。



